
Sociedad Colombiana de sarcopenia (Diciembre 2016).

1931

1996

1998

2003

2007

2010

2010

2011

2011

Sarcopenia

Sarcopenia
Medida por absorciometria dual de rayos X (DXA)3
Tiene en cuenta el Índice de Masa Muscular Apendicular (IMMA)
IMMA= Masa muscular apendicular/ Talla2 en metros (basada en 2SD por
debajo del promedio de una población joven adulta)
Criterios de Baumgartner
Mujeres: resultado menor de 5.45 Kg/m2
Hombres: resultado menor de 7.26 Kg/m2
Criterios de Kim:
Mujeres: resultado menor de 5.14 Kg/m2
Hombres: resultado menor de 7.40 Kg/m2
IMMA: Masa muscular apendicular/Talla2 en metros (20% por debajo del
promedio de una población joven adulta)
Criterios de Delmonico
Mujeres: resultado menor de 5.67 Kg/m2
Hombres: resultado menor 7.23 kg/m2
Media por Bioimpedanciometria (BIA)
Datos para bioimpedanciometro tetrapolar en posición supina.
Tiene en cuenta la masa muscular esquelética absoluta (no es masa
apendicular)
IMME: Masa Muscular Esquelética/Talla2 en metros (Basado en 2 SD por
debajo del promedio de una población joven adulta)
Criterios de Janssen
Mujeres: resultado menor de 5.75 Kg/m2
Hombres: resultado menor de 8.50Kg/m2
Bajo rendimiento:
La pérdida de la masa muscular conlleva a reducción de la fuerza, capacidad
funcional, tasa metabólica basal, equilibrio y coordinaciòn entre otras
funciones. La cuantificación de la disminución de la capacidad funcional o un
bajo rendimiento físico se puede realizar de múltiples maneras:
Cuantificación de la actividad física mediante encuestas o cuestionarios
Calorimetría directa (Gold Estándar)
Calorimetría indirecta
o Ergoespirometría
o Prueba de esfuerzo
Test de tolerancia al ejercicio
Test de banco
Test de caminata
Test de campo
Test de potencia
Test de coordinación
La base de la cuantificación objetiva de la capacidad funcional, es la aplicación
de una carga física conocida y la evaluación y comparación de la respuesta
fisiológica contra un varemos establecido por edad y género. El resultado final
puede ser dado en diferentes unidades dependiendo del biomarcador elegido
para el control:
Calorimetría directa: Kilocalorías producidas por el sujeto.
Ergoespirometrìa: Los Biomarcadores más utilizados son: VO2 pico en
mlO2 /K/min – METs – Kilocalorías – Frecuencia cardiaca
Test indirectos: pueden convertir sus resultados a los mismos
biomarcadores anteriores o sus tablas de normalidad están dadas en:
distancia (metros), en tiempo (segundo), en peso (kilos), velocidad
(m/seg), trabajo (julios) o potencia (vatios).
Se ha sugerido la cuantificación de la velocidad de marcha en 6 metros con
partida detenida o sin impulso así:
International Working Group on Sarcopenia menor a 1 m/seg
The European Working Group on Sarcopenia in Older People”
(EWGSOP) menor a 0.8 m/seg
The Special Interest Group of the European Sarcopenia Working Group
menor a 0.8 m/seg
Las recomendaciones del Grupo internacional de trabajo en sarcopenia en
cuanto a la utilización de los diferentes biomarcadores tanto en el diagnóstico
como en el seguimiento de la patología, va dirigida a la gran importancia de la
cuantificación de la función muscular y la capacidad funcional, por lo que es
aceptado cualquier test validado que lo consiga:
Test de marcha de los 6 minutos – 6MWT: riesgo en distancias menores
de 400 metros.
Pruebas de esfuerzo en banda o cicloergòmetro: riesgo con resultados
menores a 8 METs
Pruebas de escalón: riesgo con resultados menores a 8 METs
Short Physical Performance Batery -SPPB-
o Prueba de equilibrio: riesgo con resultados menores de 1 punto
o Prueba de velocidad de marcha: riesgo con resultados menores
de 2 puntos
o Prueba de levantarse de la silla: riesgo con resultados menores de
2 puntos
Get up and go Test.
Fuerza Muscular:
Existen múltiples formas de medir la fuerza muscular y se han empleado
escalas subjetivas con signos (+) cuando el músculo es capaz de contraerse,
vencer la gravedad y vencer la fuerza del examinador, hasta escalas objetivas
en las que el evaluado es capaz de vencer una resistencia o peso conocido con
halteras, discos, bandas, cauchos o poleas y técnicas mucho más sofisticadas
en la que la dinamometría se realiza de manera computarizada construyendo
curvas de torques, aceleraciones y velocidades angulares. Este proceso se
puede realizar en cualquier músculo o en diferentes grupos musculares que
realicen una misma función o sea sinérgicos. Es de esperar que el proceso de
desacondicionamiento muscular ocurra de manera más acentuada en los
grupos musculares menos empleados, dependiendo de manera lógica de la
dominancia del sujeto. Se puede medir la fuerza isométrica máxima mediante
dinamometría o la fuerza isotónica.
Existen test que miden la capacidad para sostener una carga en el tiempo,
usualmente 1 minuto en la cual se realizan repeticiones de movimientos con
autocargas de grupos musculares importantes como los abdominales, flexo-
extensores de hombro y codo y flexo extensores de rodilla y cadera.
Teniendo en cuenta que los grupos investigadores de sarcopenia son
“Geriatras” y “Gerontólogos” e iniciaron sus estudios en poblaciones de
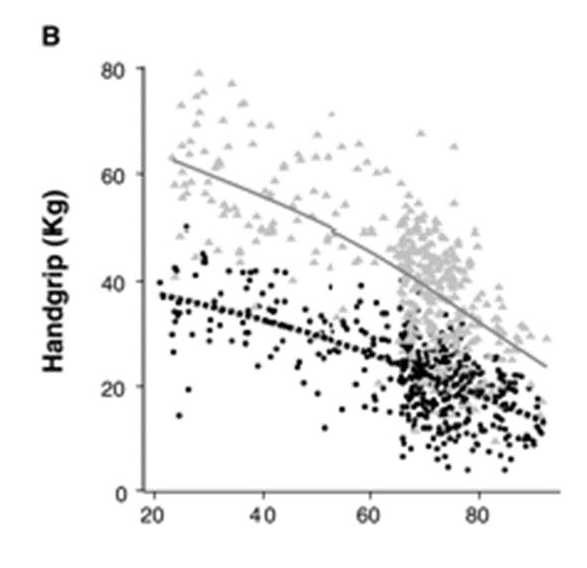
adultos mayores, el test elegido desde entonces fue la medición de la fuerza
de aprensión del mano medido con un dinamómetro, cuyos puntos de corte
fueron:
Hombre anormal < 30 Kg
Mujer anormal < 20 Kg
Comenzando a la edad de los 30 años los individuos pierden 1% de su masa
muscular cada año y a la edad de 80 años, se ha perdido entre 30 a 50% de la
masa muscular. Esto hace que la prevalencia esté estimada entre el 10 al 25%
dependiendo de la población y del método usado para medirla, y en los
octogenarios la prevalencia es casi del 50% 4.
Fuerza Muscular:
Existen múltiples formas de medir la fuerza muscular y se han empleado escalas subjetivas con signos (+) cuando el músculo es capaz de contraerse, vencer la gravedad y vencer la fuerza del examinador, hasta escalas objetivas en las que el evaluado es capaz de vencer una resistencia o peso conocido con halteras, discos, bandas, cauchos o poleas y técnicas mucho más sofisticadas en la que la dinamometría se realiza de manera computarizada construyendo curvas de torques, aceleraciones y velocidades angulares. Este proceso se puede realizar en cualquier músculo o en diferentes grupos musculares que realicen una misma función o sea sinérgicos. Es de esperar que el proceso de desacondicionamiento muscular ocurra de manera más acentuada en los grupos musculares menos empleados, dependiendo de manera lógica de la dominancia del sujeto. Se puede medir la fuerza isométrica máxima mediante dinamometría o la fuerza isotónica.
Existen test que miden la capacidad para sostener una carga en el tiempo,
usualmente 1 minuto en la cual se realizan repeticiones de movimientos con autocargas de grupos musculares importantes como los abdominales, flexo-
extensores de hombro y codo y flexo extensores de rodilla y cadera. Teniendo en cuenta que los grupos investigadores de sarcopenia son
“Geriatras” y “Gerontólogos” e iniciaron sus estudios en poblaciones de
adultos mayores, el test elegido desde entonces fue la medición de la fuerza de aprensión del mano medido con un dinamómetro, cuyos puntos de corte fueron:
Hombre anormal < 30 Kg
Mujer anormal < 20 Kg
Comenzando a la edad de los 30 años los individuos pierden 1% de su masa
muscular cada año y a la edad de 80 años, se ha perdido entre 30 a 50% de la masa muscular. Esto hace que la prevalencia esté estimada entre el 10 al 25% dependiendo de la población y del método usado para medirla, y en los octogenarios la prevalencia es casi del 50% 4.
Sobre los costos al sistema Janssen y colaboradores estiman que la sarcopenia genera un exceso de gastos al sistema de atención de salud de los Estados Unidos un costo superior de $18.4 mil millones de dólares al año (año 2001), debido a la discapacidad asociada.
Aquí algunas tablas sobre la variación en incidencia y prevalencia de la entidad, las cuales varían por la falta de unificación de criterios diagnósticos, aún con el trabajo de los grupos mundiales.
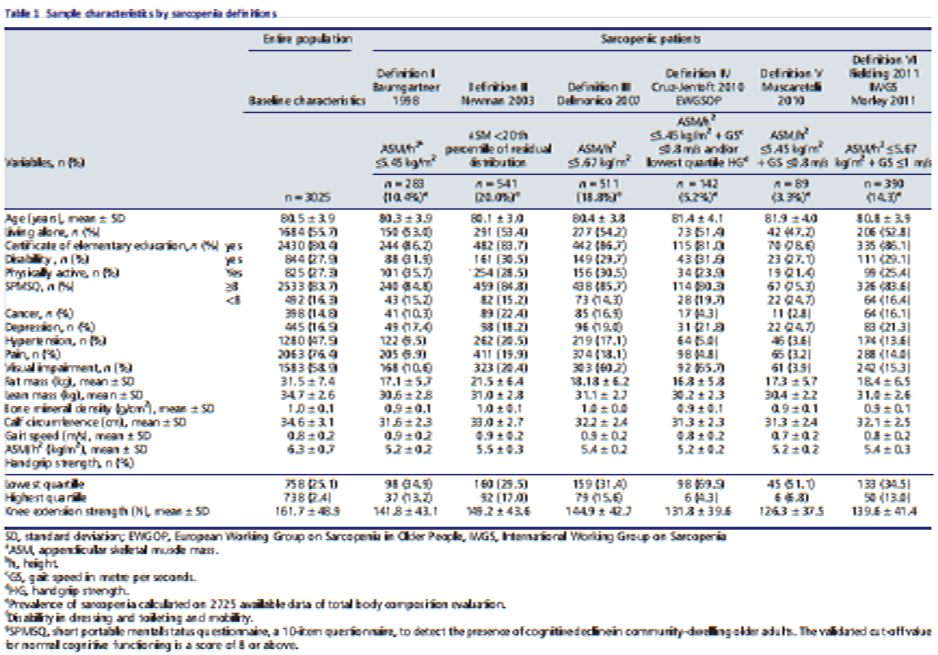
En Bogotá Samper y colaboradores (2016) encontraron una prevalencia de 11.5% en la población adulta mayor utilizando otros criterios diagnósticos.
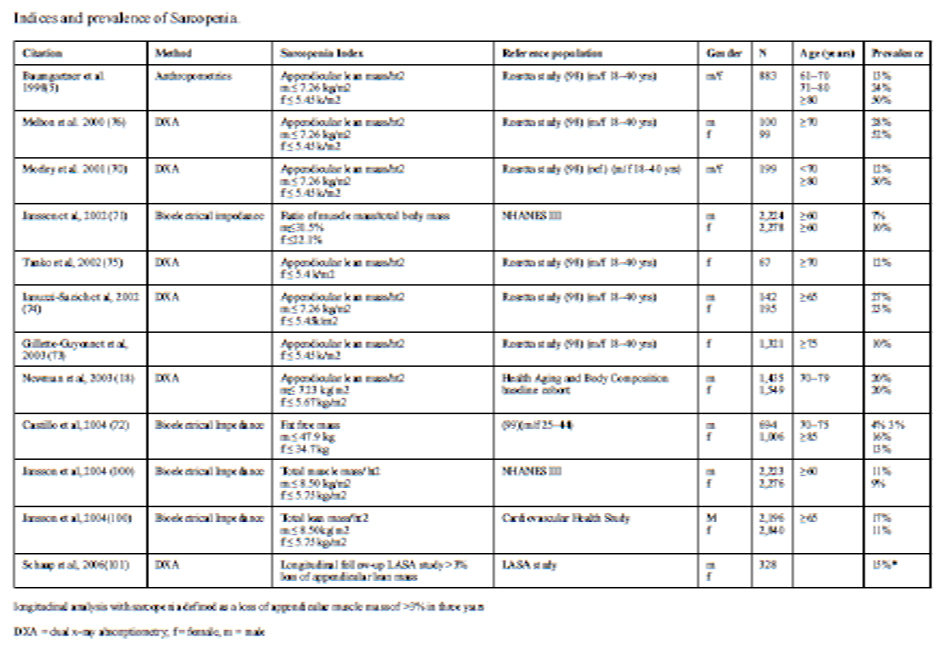
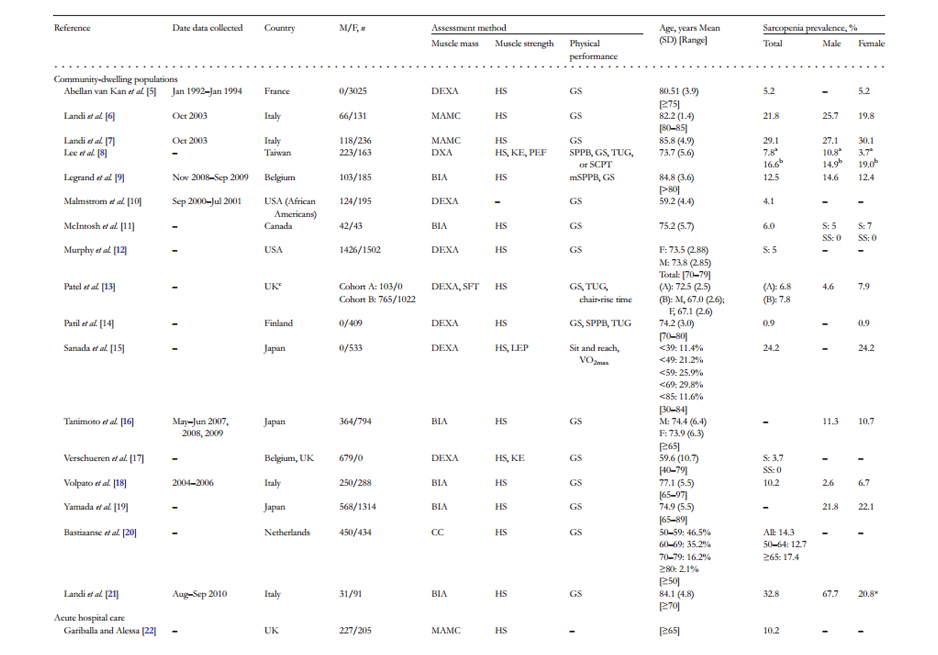
De acuerdo al estudio EPIDOS, la prevalencia se extendió de 3,3 (IC del
95%, 2,6-4, Propuesta V de Muscaretoli) -20,0% (IC del 95%, 17,3-20,3,
Propuesta III de Delmonico), Existe una gran superposición entre las seis
definiciones, pero sólo 85 participantes (3,1%) coinciden con las seis
definiciones de Sarcopenia.
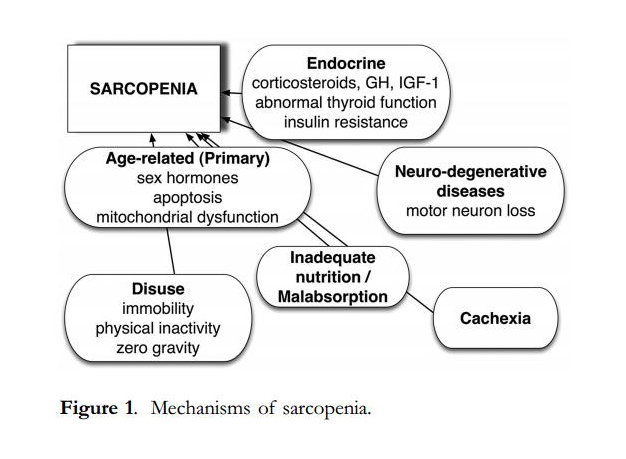
Fisiológicamente se caracteriza por ser una entidad multifactorial,
presentando un amplio sustrato de situaciones precipitantes y usualmente
(más no únicamente) asociado a los cambios de la adultez mayor,
representada en el siguiente esquema:
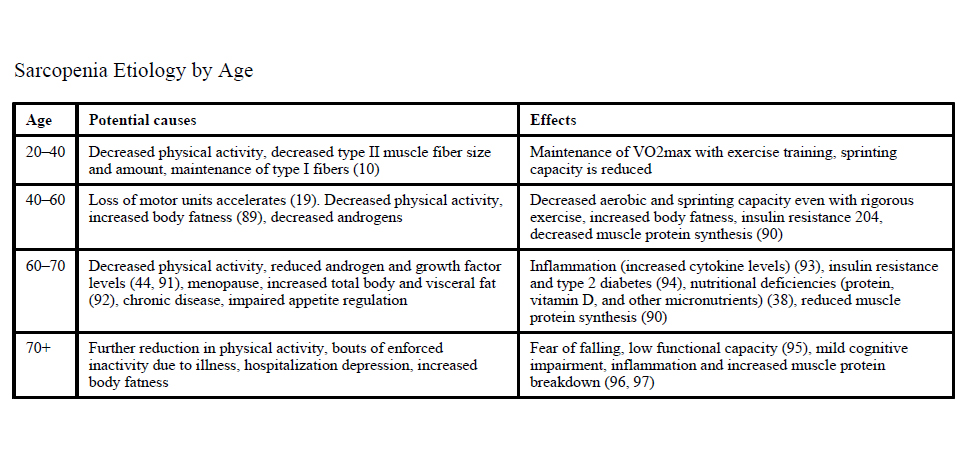
Lo que varía según el grupo etáreo:
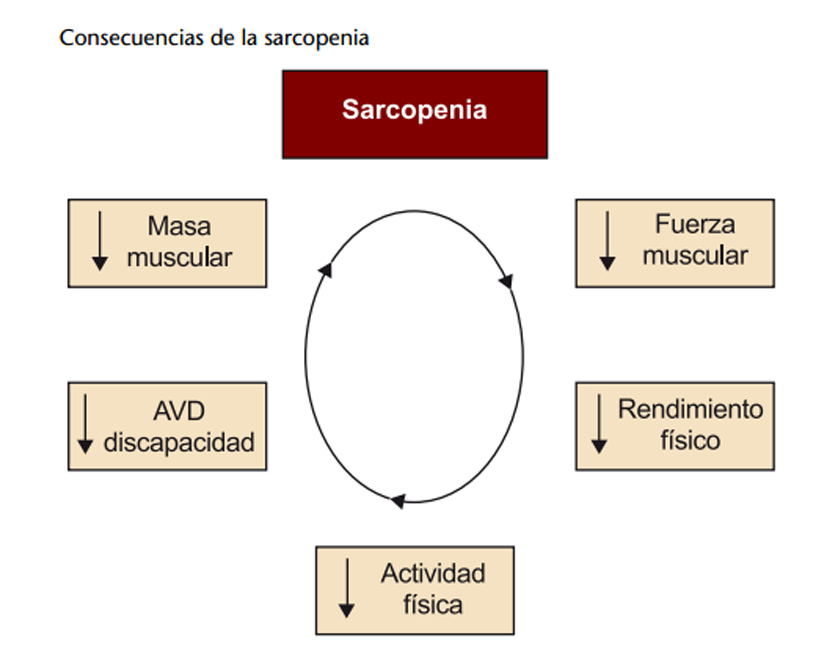
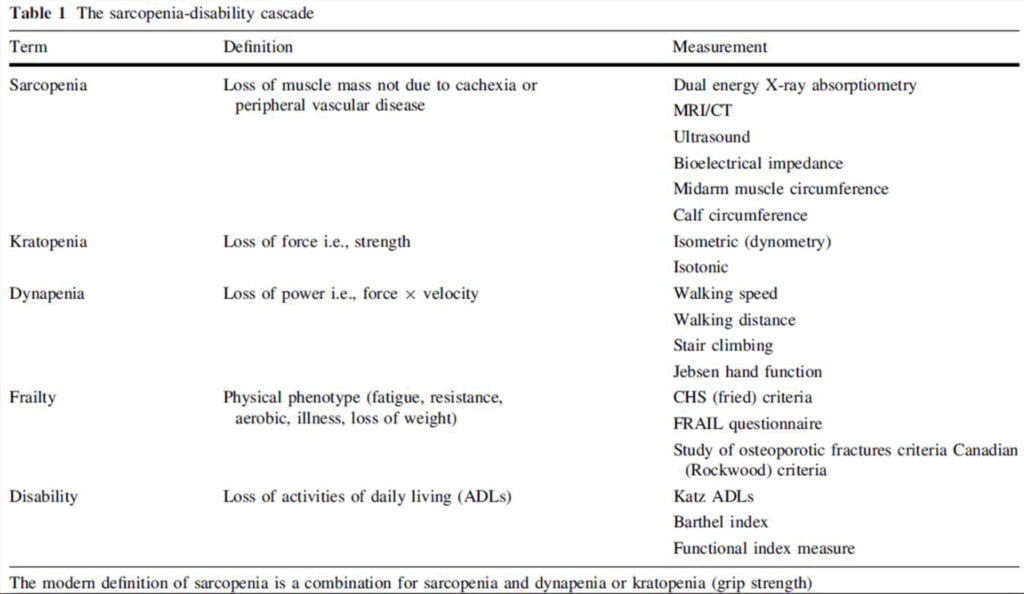
La cascada clínica de la enfermedad se ha descrito de la siguiente manera:

De manera que se perpetúa la entidad en una mecánica de bola de nieve:
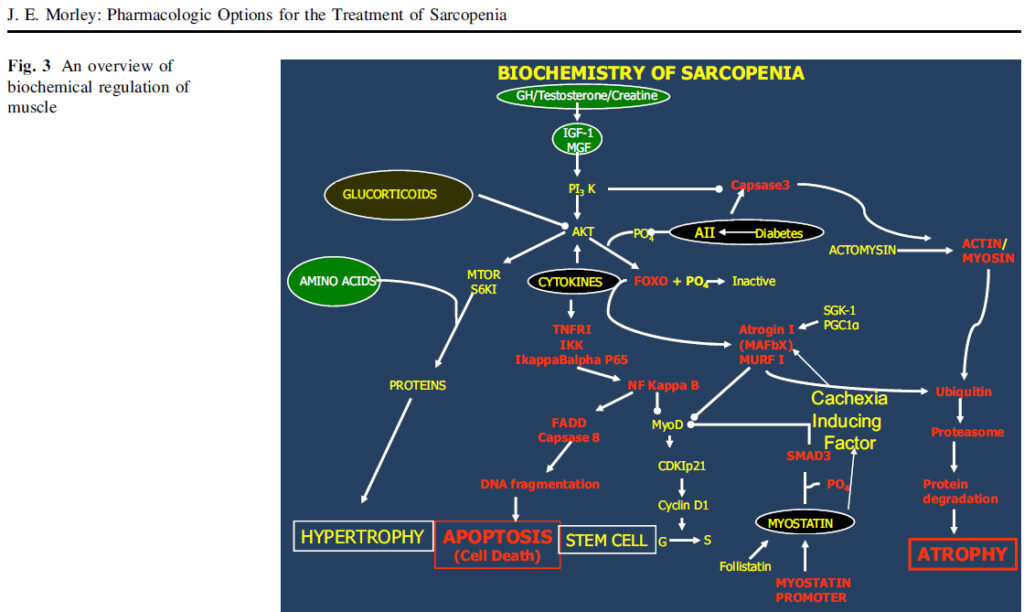
Con los avances que se realizan progresivamente en la tecnología, se ha podido realizar una ampliación sobre los fenómenos bioquímicos que facilitan o dificultan el desarrollo de la entidad, Morley y colaboradores han estudiado el esquema bioquímico de la sarcopenia (esquema adelante), ésta entidad resulta de una disminución desproporcionada en la síntesis de proteínas del músculo esquelético y / o un aumento de la degradación de proteínas del músculo esquelético. Las hormonas anabólicas y la actividad muscular conducen el sistema mediante la activación del sistema fosfatidilinositol 3 quinasa / AKT serina-treonina quinasa. Mayor disponibilidad de aminoácidos, en particular, aminoácidos de cadena ramificada estimulan mTOR. Este sistema estimula la síntesis de proteína muscular a través de la activación de la diana de mamífero de la rapamicina (mTOR) e inhibe la atrofia fosforilando la proteína FOXO. La FOXO fosforilada se inactiva por lo tanto reduce la expresión de la ligasa E3, atrogina I y, posteriormente, previene de la degradación de proteínas por el sistema de ubiquitina-proteasoma. Una mayor expresión de MuRF-1 y atrogina-1 de expresión se ha observado en el músculo de roedor de edad en comparación con joven junto con un nivel de 90% más alto de conjugados de ubiquitina. Los niveles elevados de angiotensina II inhiben la fosforilación de FOXO y estimulan la caspasa 3, que escinde actomiosina, permitiendo que la actina y la miosina a ser degradados por el sistema de ubiquitina –proteasoma. Los glucocorticoides inhiben la actividad de AKT. La miostatina D inhibe el ciclo celular a través de SMAD3 y MyoD, inhibiendo así la producción de células satélite mientras que la testosterona aumenta la producción de células satélite mediante la estimulación de β- catenina. Las citoquinas causan la fragmentación del ADN y la apoptosis mediante la estimulación de NFkB para producir la caspasa 8. Hay pocos datos comparando la expresión de factores de músculo esquelético humano afectan a la expresión del sistema ubiquitina-proteasoma, un reciente estudio examinó las características basales de las mujeres jóvenes (23 ± 2y) y mayores (85 ± 1a), así como su respuesta a un ejercicio de resistencia. Al inicio del estudio, las mujeres mayores expresaron FOXO3A y MuRF-1 genes en niveles más altos que lo hizo a las mujeres jóvenes. En respuesta a una serie de ejercicios de resistencia a todas las mujeres demostraron un aumento sustancial en la expresión de MuRF-1, sin embargo, las mujeres de edad también mostraron una mayor expresión de atrogina-1, indicando tal vez una mayor respuesta proteolítica músculo al hacer ejercicio.
Los médicos deben sospechar la Sarcopenia en los pacientes que presentan:
De acuerdo al estudio EPIDOS CON Respecto a las diferentes dificultades
autoinformadas en la función física, el 3,7% coincidió con dificultades
para caminar, el 40,9% tiene dificultad en subir escaleras, el 51,2% tiene
dificultades en escaleras descendentes, el 39,5% tiene problemas de silla
y el 48,5% tiene más de tres dificultades. El poder predictivo de cada
modelo de referencia varió entre 68% y 81%. Todas las definiciones de
sarcopenia se asociaron significativamente con estos elementos
«escaleras descendentes» y «dificultades de movimiento».
Los criterios de diagnóstico se acuñan en 3 grupos:
Los médicos deben sospechar la Sarcopenia en los pacientes que presentan:
De acuerdo al estudio EPIDOS CON Respecto a las diferentes dificultades
autoinformadas en la función física, el 3,7% coincidió con dificultades
para caminar, el 40,9% tiene dificultad en subir escaleras, el 51,2% tiene
dificultades en escaleras descendentes, el 39,5% tiene problemas de silla
y el 48,5% tiene más de tres dificultades. El poder predictivo de cada
modelo de referencia varió entre 68% y 81%. Todas las definiciones de
sarcopenia se asociaron significativamente con estos elementos
«escaleras descendentes» y «dificultades de movimiento».
Los criterios de diagnóstico se acuñan en 3 grupos:

Y el esquema de diagnóstico hasta el momento ha sido el siguiente:
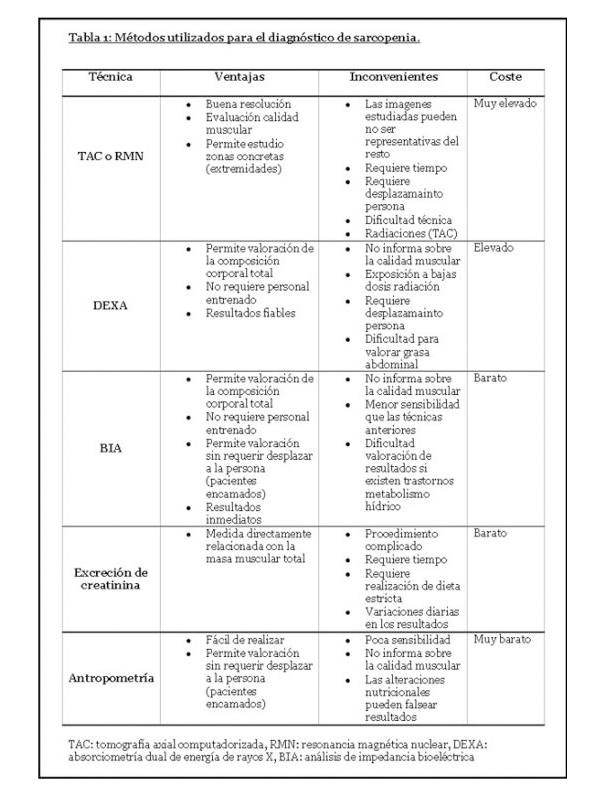
Los indicadores de composición corporal se acuñan en la siguiente tabla:
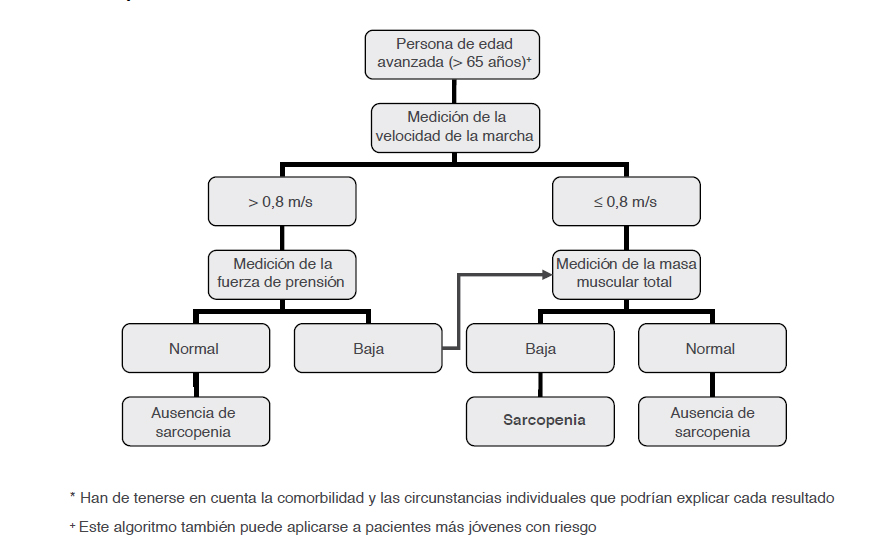
Pudiendo realizar una diversificación del diagnóstico de acuerdo al escenario clínico presentado, resumido de la siguiente manera:
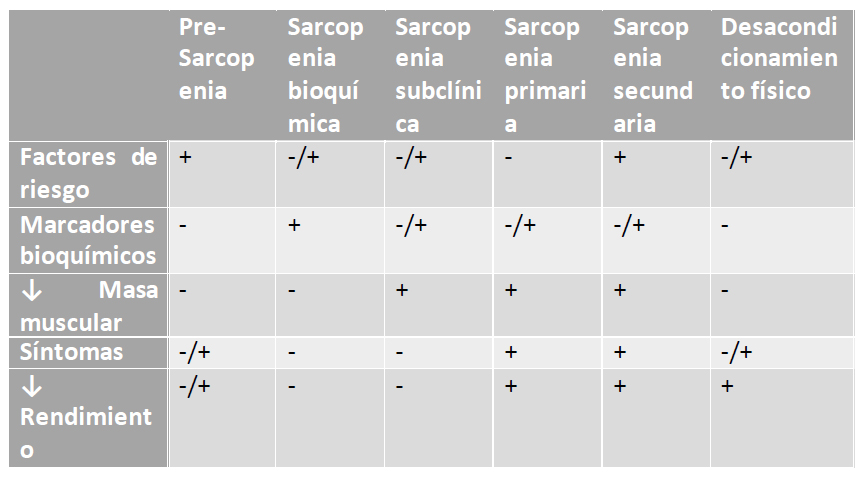
El estudio EPIDOS permite entender que las medidas de rendimiento
físico y de masa parecen no ser más relevantes que la definición basada
en la masa muscular sólo en la predicción de dificultades físicas. Ninguna
de las seis definiciones de sarcopenia exploradas parecía superior a la
otra. En otras palabras, la sarcopenia, cualquiera que sea la definición
utilizada, no mejoró significativamente la predicción de las dificultades
físicas autoinformadas.
La “Sarcopenia” un síndrome caracterizado por la pérdida progresiva y
generalizada de la cantidad y la calidad de masa muscular esquelética con
incremento del riesgo de discapacidad física, enfermedades crónicas no
transmisibles, reducción de la calidad de vida y muerte.
La sarcopenia es una condición prevenible y reversible.
Se considera “Sarcopenia primaria”, aquella pérdida muscular producto
exclusivamente del envejecimiento y “Sarcopenia secundaria” la pérdida
muscular como consecuencia de la inactividad física o enfermedad que
impacte en la estructura o metabolismo muscular o condiciones que altere el adecuado aporte nutricional.
Son causas de Sarcopenia secundaria:
Por inactividad física
o Sedentarismo
o Desacondicionamiento físico
o Reposo en cama o postración
Por enfermedad
o Enfermedades inflamatorias
o Neoplasias
o Enfermedades endocrinas
o Enfermedades neurodegenerativas
o Fracaso orgánico avanzado
Por aporte nutricional
o Dieta inadecuada
o Enfermedades digestivas
o Malabsorción
o Anorexia por fármacos
Teniendo en cuenta que la Sarcopenia posee dos componentes estrechamente
relacionados, pero no directamente proporcionales como son la cantidad de
músculo y su calidad y que adicionalmente la presencia de síntomas es un
estadio tardío de pérdida de la función, es posible encontrar grados, tipos oniveles de sarcopenia.
Presarcopenia: condición de salud anterior a la aparición de la sarcopenia, en la cual existen factores de riesgo o causas de sarcopenia secundaria, se evidencia pérdida de la masa muscular pero la calidad del músculo es aceptable para la edad. Pueden expresarse síntomas, pero no se evidencian biomarcadores húmedos ni secos para función muscular.
Sarcopenia Subclínica: condición de salud en la cual existen factores de riesgo o causas de sarcopenia secundaria y síntomas de pobre calidad muscular que se evidencian mediante biomarcadores secos o criterios de alteración de la función mecánica o metabólica del músculo y biomarcadores húmedos sin el hallazgo de pérdida de masa muscular.
Sarcopenia Bioquímica: estado de salud en la que existen factores de riesgo o causas de sarcopenia secundaria, síntomas de pobre calidad muscular con evidencia de biomarcadores húmedos o bioquímicos, pero sin evidencia objetiva de pérdida de masa muscular o reducción de la calidad del músculo.
FACTORES DE RIESGO:
Edad: Mayores de 65 años
Habito nutricional: Dieta baja en proteína < 1 g/k/dìa Hábito de actividad física: Sedentario > 8 horas/dìa sedente (1.5 METS)
Nivel de actividad física: Inactivo < 2 METS promedio hora/ dìa Antecedentes de enfermedades crónicas
Hospitalización prolongada
Historial de caídas
SINTOMAS:
Kratopenia o debilidad muscular
Dinapenia o pérdida de la potencia muscular o velocidad de ejecución
Intolerancia al ejercicio
Pérdida inexplicable de peso
BIOMARCADORES HUMEDOS
Hormona de crecimiento
Testosterona
IGF 1
Cortisol
Insulina – HOMA
CPK
Urea
Miostatina
ILK 6
BIOMARCADORES SECOS
Test de fuerza: Kilogramos – Libras – Newtons
Test de potencia: velocidad – vatios
Test de coordinación y equilibrio
Test cardiopulmonares
o VO2 màx. Consumo de oxigeno pico o máximo
o Frecuencia cardiaca máxima
o Umbral aeróbico / anaeróbico
o Umbral ventilatorio
Las características propias de los componentes diagnósticos de la sarcopenia,
como su método de cuantificación permiten que se puedan medir
objetivamente por separado y serán clasificadas como criterios diagnósticos.
Son criterios diagnóstico mayores los relacionados a la masa muscular y
criterios diagnósticos menores los relacionados con la función; dentro de esta
categoría se determinó definir criterios diagnósticos menores tipo A que
correspondela cuantificación de la función mecánica y metabólica del músculo
a partir de biomarcadores secos o alteración de la estructura o arquitectura
muscular de acuerdo a la biopsia muscular y criterios diagnósticos menores
tipo B a la cuantificación de los diferentes biomarcadores húmedos
relacionados con la función muscular.
Ante un paciente con factores de riesgo o cualquier síntoma muscular descrito
se debe iniciar la búsqueda de caso con la batería para “Sarcopenia”.
El diagnostico de Sarcopenia se realizará con mínimo:
1 criterios MAYOR + 1 criterio MENOR A
1 criterio MAYOR + 1 síntoma + 1 criterio MENOR B
1 criterio MAYOR + 2 o más criterios MENORES B
CRITERIOS MAYORES:
La medición de la masa muscular se debe realizar de dos formas, la más rápida
y económica mediante bioimpedanciometria con aparatos tetra polares
siguiendo los criterios propuestos por Janssen para calcular el IMME o
mediante la medición de la masa muscular apendicular utilizando DXA
siguiendo los criterios propuestos por Baumgartner para calcular el IMMA:
CRITERIOS MENORES A:
El diagnóstico de Presarcopenia se realizará con:
1 criterio MAYOR + síntoma
Sin evidencia de disminución de la función / Biomarcadores (-)
El diagnóstico de Sarcopenia Subclínica se realizará con:
1 criterio MENOR + síntoma
Sin evidencia de disminución de la masa muscular
El diagnóstico de Sarcopenia Bioquímica
2 o más criterios MENORES B

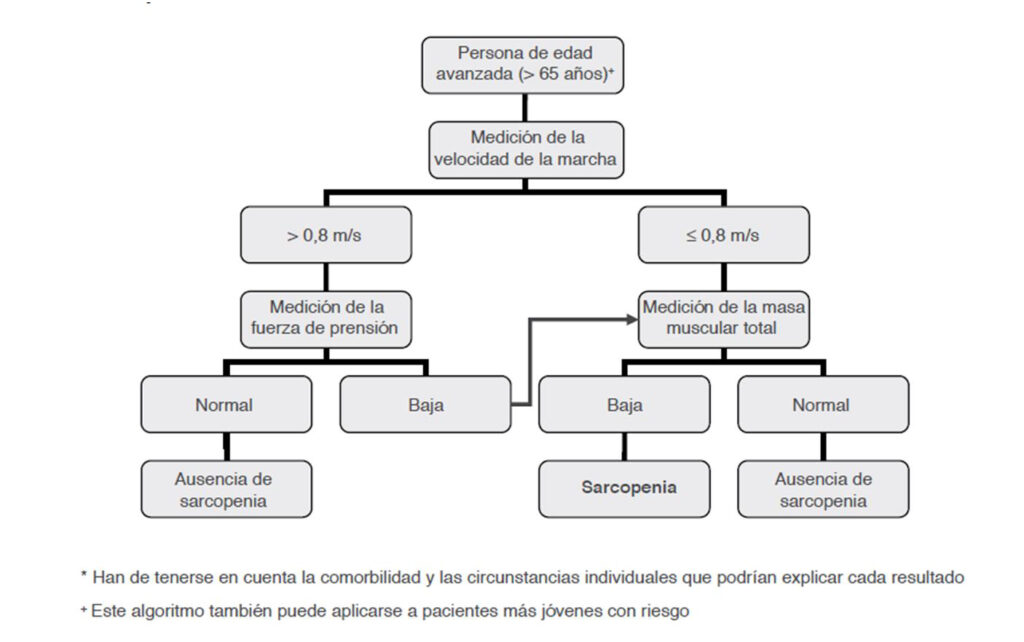
Las alternativas terapéuticas se resumen en la siguiente tabla:
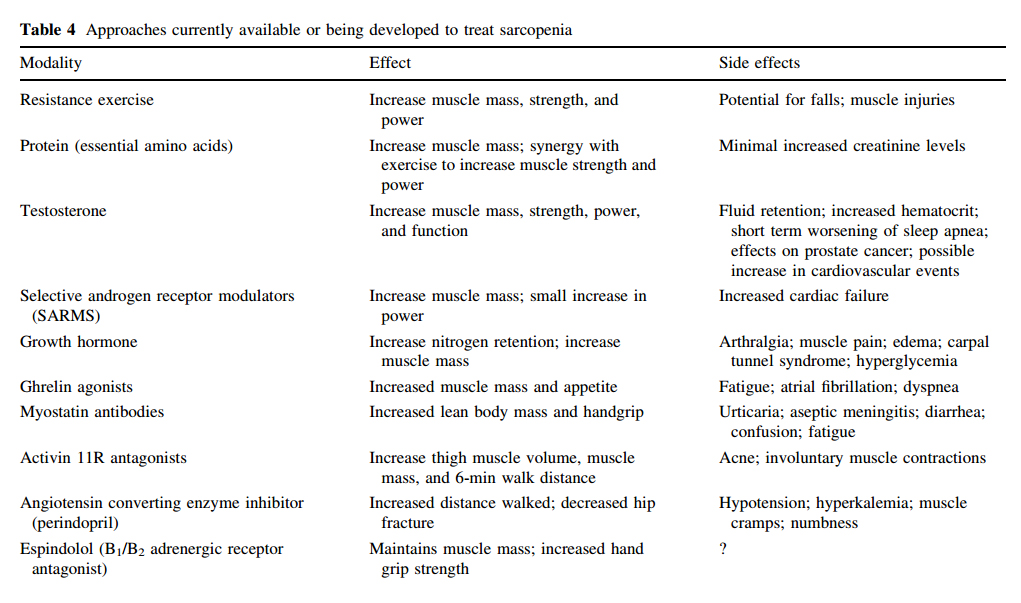
Las alternativas terapéuticas se resumen en la siguiente tabla:
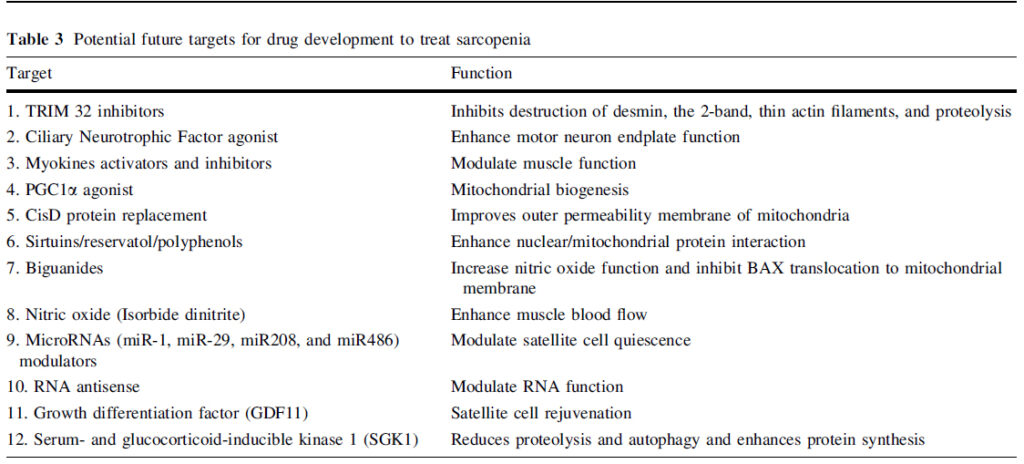
La sarcopenia representa una causa importante de discapacidad y el aumento
de los costos de salud en las personas mayores. Si bien es muy común, como
la mayoría de los síndromes geriátricos, pocas veces reconocido por los
médicos, ahora entendiendo también que no es exclusivo de la población
adulta mayor. Identificación de pacientes sarcopénica en mayor riesgo se
puede realizar utilizando una herramienta fácil de realizar la evaluación de la movilidad, como la velocidad de la marcha y las medidas comúnmente
obtenidas de la composición corporal. DXA instrumentos se utilizan para
evaluar la densidad ósea para la identificación de los grupos de mayor riesgo para el desarrollo de la osteoporosis. Los avances en la instrumentación y software permiten una medida exacta y precisa de la masa libre de grasa en las personas de edad avanzada. Las personas mayores (>65 años) deben ser examinadas para tamizaje: la disminución de la masa muscular y baja capacidad funcional. Estas personas tienen un alto riesgo de pérdida de la independencia y la muerte prematura. Una serie de tratamientos prometedores para la sarcopenia están actualmente bajo investigación incluyendo la actividad física, las terapias nutricionales, terapia con andrógenos, y otras estrategias conductuales y farmacológicas. Sin embargo, hasta las organizaciones profesionales, y los Centros especializados para la atención en salud reconozcan la sarcopenia como una entidad/condición clínica su identificación, tratamiento y el desarrollo continuo de posibles agentes «anti-sarcopenia» será limitado.
Doctor Irving H. Rosemberg MD Universidad de Harvard – Internista y Gastroenteròlogo, Actualmente Profesor de la Universidad Jean Mayer de la Universidad de Tufts, Profesor de Nutriciòn de la Escuela Frietman de Nutriciòn, Cientìfico Senier y Director Interino del Laboratorio de Neurociencias y Envejecimiento. [email protected] (617)6363701
Doctor William J. Evans PhD Zoologo – Biologo. Adjunct Professor in the geriatric program at the Duke University. President, Muscle & Health Division, KineMed, Inc. (Enfocado en la ingesta de proteínas en sarcopenia) Desde 1982 trabaja en la rehabilitación geriátrica en la Universidad de Arkansas y Tuft.
Doctor Richard N Baumgartner PhD in Nutritional Epidemiology from University of Texas (1982). The principal investigator in “New Mexico aging process study” (1998-2004). Actualmente Profesor of epidemiology of University Lousville.
Doctora Anne B. Newman Geriatric of Presbyterian University Hospital, Pittsburgh. Public
Health Public.
Doctor Alfonso J. Cruz-Jentof Mèdico geriatra de la Universidad Complutense de Madrid.
Director de la unidad de geriatrìa del Hospital Ramòn y Cajal.
© 2023 Created with Royal Elementor Addons